Lorsque nous entendons le mot « régénération », nous imaginons d’emblée la repousse spontanée d’organes ou de membres perdus comme on le voit dans les films de science-fiction et autres comics dédiés aux super-héros tel Wolverine dont le pouvoir auto-guérisseur est la marque de fabrique…
Dans la vie réelle, la situation semble moins idéale et nous partons généralement du principe que le corps humain ne se régénère pas. Un bras amputé ne repousse pas, une lésion de la moelle épinière peut entraîner une paralysie à vie et une dent arrachée est perdue à jamais. Notre corps se couvre de cicatrices, un patient peut être condamné à se déplacer en fauteuil roulant ou à attendre une greffe d’organe pour avoir une chance de survivre.
On a donc l’impression d’être coincé dans un corps incapable de s’auto-réparer en cas de blessure grave. Pourquoi en est-il ainsi ? Et la médecine du futur pourra-t-elle un jour aider à régénérer ces parties perdues ?
Un corps en fait en constant renouvellement
Pourtant, à l’opposé de ces idées reçues démoralisantes, notre corps cumule les prouesses biologiques ! Loin des regards, la plupart de nos organes se renouvellent constamment en éliminant les cellules anciennes ou mortes et en les remplaçant par de nouvelles afin de rester dans un état optimal.
Notre peau, par exemple, perd des millions de cellules par jour qui sont en permanence remplacées. Grâce à ce rythme soutenu, vous retrouvez, tous les mois environ, une nouvelle couche de cellules cutanées. C’est pourquoi griffure, estafilade et coupure guérissent spontanément – ne vous coupez pas trop profondément, quand même.
Les organes internes subissent également ce genre de « rajeunissement ». Les cellules qui tapissent l’intérieur de votre estomac se régénèrent en continu pour résister à leur environnement acide. Vous changez du coup la paroi de votre estomac toutes les semaines. Le tissu osseux est, lui, entièrement remplacé tous les 10 ans et, en cas de fracture, de nouvelles cellules osseuses recollent obligeamment les deux parties.
Après avoir livré une bataille épuisante contre des micro-organismes envahisseurs, notre système immunitaire régénère aussi les cellules perdues pour retrouver sa composition originale.
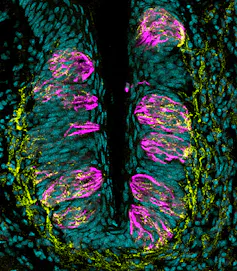
Les papilles gustatives de la langue (rose) détectent les goûts et saveurs et les transforment en signaux électriques envoyés au cerveau par les fibres nerveuses (jaune). En cas de blessure, les bourgeons gustatifs peuvent se régénérer en 10 jours et fonctionner à nouveau. Dany Gaillard et Linda Barlow/Université du Colorado, Author provided
Mais l’organe humain le plus impressionnant en termes de régénération est le foie. Son rôle de détoxification du sang l’y oblige… En cas de dommage grave ou d’amputation partielle, il est capable de repousser et fonctionner à nouveau comme si de rien n’était. Et l’on peut multiplier les exemples… Avez-vous déjà pensé à votre langue, dont les papilles gustatives sont régulièrement victimes de brûlures causées par la précipitation ? Dix jours seulement leur suffisent pour se reconstituer et vous permettent de goûter (littéralement) à nouveau au plaisir de la cuisine.
Quelques limites toutefois…
Mais si le corps est capable de remplacer autant de tissus, pourquoi alors vieillissons-nous ? Tout d’abord, parce que lorsque nous prenons de l’âge, les cellules accumulent des dommages – dans leur matériel génétique notamment. Ces « nouvelles cellules » qui naissent tard dans notre vie, si l’on peut dire, ne bénéficient pas d’un bel ADN tout neuf de nouveau-né : elles disposent, comme leurs consœurs, de l’ADN endommagé de leurs cellules mères.
Et une fois un certain seuil d’altérations accumulées atteint, une cellule ne peut plus fonctionner. Ce phénomène est comme une horloge inéluctable qui nous amène chaque jour un peu plus vers notre date d’expiration.
Deuxièmement, certains tissus ou organes ne se régénèrent jamais (entièrement). C’est, malheureusement, le cas du cerveau. Les cellules nerveuses, par exemple, qui font fonctionner notre corps et notre esprit, ne repoussent jamais en cas de blessure. Tout comme leur propriétaire, elles reposent en paix après des décennies de travail.
Enfin, lorsque la blessure d’une partie du corps est trop importante, sa réparation complète devient impossible. Par conséquent, même si le corps humain peut régénérer certaines de ses parties, il ne peut pas remplacer toutes ses pièces cassées comme on le ferait pour une voiture.
Éponges et salamandre, les championnes de la régénération au naturel
D’où viennent ces limites ? L’évolution ne pourrait-elle pas sélectionner de telles caractéristiques pour favoriser la survie ? Force est de reconnaître que certains animaux font des miracles…

Ce petit animal marin, Hydra vulgaris, a été (bien) nommé d’après l’hydre de Lerne de la mythologique grecque, et dont les têtes repoussaient au fur et à mesure qu’Hercule les tranchait. Proyecto Agua, Author provided
Un peu moins éloigné de nous dans l’arbre du vivant, le poisson-zèbre, modèle animal populaire dans les laboratoires, n’est pas en reste puisqu’il peut faire repousser ses nageoires caudales, des parties de son cerveau, son cœur et de nombreux autres organes.

Cette salamandre a perdu sa queue récemment, et est en train de la régénérer. Greg Schechter/Flickr, Author provided
Les salamandres, enfin, sont tout aussi douées. Si vous avez déjà essayé d’en attraper une par la queue, vous vous êtes sans doute retrouvé avec seulement cet appendice caudal frétillant dans les doigts. Elle s’en sera débarrassée sans regret et en arborera un nouveau en l’espace de quelques semaines seulement !
Pas de miracle toutefois. Plus on monte dans l’échelle de l’évolution, plus les capacités de régénération se réduisent. Coupez un poisson-zèbre en deux et il ne se passera rien de bon pour lui. Les souris ne réparent pas plus une lésion cérébrale grave ou un membre perdu que les êtres humains.
Retour vers la cellule souche…
Pourquoi les animaux « plus simples » (quoiqu’en se référant à ce trait, on pourrait dire plus complexes !) se régénèrent-ils si bien – et pas nous ?
Une grande partie de l’histoire tient à un groupe de cellules bien particulier : la cellule souche. Immature, elle peut se transformer en n’importe quel type de cellule, de foie, de peau, de cerveau ou de rein, lorsqu’elle reçoit le signal adéquat et les bonnes instructions.
Et il existe plusieurs sortes de cellules souches chez les animaux. Certaines peuvent former tous les types de cellules du corps de leur propriétaire : ce sont des cellules « pluripotentes », comme chez Hydra. Celles que les scientifiques trouvent chez les vertébrés adultes ne peuvent plus donner naissance qu’à quelques types cellulaires : elles sont dites « multipotentes ».
Chez les salamandres, en cas de blessure, des cellules souches se rassemblent dans le bourgeon de la plaie et commencent à reconstruire à l’identique le membre perdu. Pour ce faire, elles utilisent le « plan » du membre, codé par les gènes. Ce n’est pas surprenant, car l’ADN niché dans chacune (ou presque) de nos cellules a déjà eu ce rôle de plan général, lors de l’embryogenèse !
Ainsi, pour reconstruire un nouveau membre à partir de zéro, il convient de réactiver précisément les bons gènes, un peu comme un architecte se plongerait dans les plans originaux d’une maison pour reconstruire un mur endommagé. Étant donné que nous partageons la majeure partie de notre ADN avec des organismes capables de se régénérer, l’identification de ces gènes « régénérateurs » et la recherche de moyens de neutraliser les freins moléculaires afin de réussir à les activer à volonté constituent un objectif majeur de la recherche sur la régénération.
Il convient également de conserver les instructions visant à prévenir toute croissance excessive et la formation de tumeurs… Les cellules souches sont capables de générer juste ce qu’il faut de cellules pour faire une copie de taille parfaite de la partie du corps perdue. Des signaux extérieurs aux cellules servent probablement à leur indiquer quand s’arrêter. Ils restent pour l’heure difficiles à identifier.
Quand l’évolution dit stop
Voici une première explication possible à notre capacité limitée : les mécanismes à gérer sont devenus si complexes au cours de l’évolution, qu’il est devenu trop difficile d’harmoniser la myriade de gènes et de signaux. Et les risques de provoquer la formation de tumeurs trop grands. Si bien que la sélection naturelle les a progressivement réduits au silence, une fois qu’un animal a atteint le stade adulte.
Il y aurait simplement trop de consignes à suivre pour exécuter encore sans risque le programme « comment se régénérer ».
Une autre raison plausible est que nous avons moins de cellules souches pluripotentes (actives) que ces autres animaux plus simples. Bien que nous en ayons. Les scientifiques essaient maintenant de comprendre ce qui se passe dans ces cellules souches lorsqu’une partie du corps est amputée chez l’Homme, par rapport aux poissons ou aux grenouilles qui font mieux que nous.
Si les chercheurs parviennent à décrypter les mécanismes chez ces animaux, ils pourraient peut-être inhiber la cicatrisation et ressusciter ce système d’autoguérison en sommeil chez nous à l’aide d’un simple cocktail de médicaments ? Ou d’outils d’édition génétique, capables de modifier à volonté l’activité de certains gènes, conçus comme des « interrupteurs de régénération » ?
Médecine régénérative : où en sommes-nous ?
Le développement de nos connaissances médicales nous donne toujours plus d’outils pour aider notre corps à se guérir.
Les chirurgiens peuvent transplanter à peu près de tout, peau, main, cornée ou cœur – voire cœur de porc génétiquement modifié pour être « humanisé » !.
Il est même désormais possible d’imprimer en 3D des organes relativement simples comme la vessie, ce qui constitue un cas de régénération artificielle en dehors du corps.
Une autre technologie révolutionnaire concerne les bras et les jambes bioniques qui peuvent être commandés par la pensée de la personne.
Mais on parlait plus de réparation sinon de remplacement que de remise en route de nos capacités ancestrales d’auto-régénération.
Une autre technique encore en phase expérimentale, mais qui s’appuie cette fois davantage sur notre capacité de régénération, est la transplantation de cellules souches.
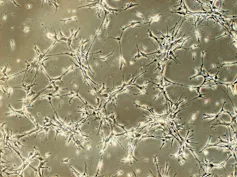
En laboratoire, on peut déjà faire pousser des cellules souches capables de générer de nouvelles cellules nerveuses et de la glie (cellules de soutien). L’espoir est de réussir un jour leur transplantation au niveau d’une blessure pour faciliter la régénération des tissus. Yirui Sun, Author provided
L’idée est simple : cultiver des cellules souches provenant d’autres parties du corps ou multipliées en laboratoire, les reprogrammer génétiquement si nécessaire, les transplanter dans le tissu blessé et administrer un cocktail de médicaments qui leur permettra de produire les types de cellules spécialisés nécessaires pour restaurer la zone endommagée. Bref, de régénérer le site en y amenant une armada de cellules souches pour qu’elles y fassent leur office. Les expériences sur les animaux sont prometteuses (et la technique fonctionne bien chez l’humain pour les greffes de moelle osseuse), mais le succès reste mitigé pour notre espèce.
Enfin, les scientifiques tentent de libérer le potentiel de réparation de nos cellules souches – par divers traitements ou demain par génie génétique. Cela serait particulièrement pertinent pour le cerveau, sujet à des maladies neurodégénératives pour lesquelles les options chirurgicales ou thérapeutiques sont limitées. Cependant, la population de cellules souches cérébrales est petite… et surtout inactive. Nous n’avons pas encore trouvé la bonne recette pour réveiller cette pourtant prometteuse équipe interne de microchirurgiens.
Pour l’instant, nous devons donc nous contenter des outils que la nature nous a donnés… Et reconnaître humblement que, en matière de régénération, nous ne pouvons pas (encore) rivaliser avec la plupart de nos minuscules confrères réputés « primitifs » !![]()
Pieter Vancamp, Post-doctorant, Muséum national d’histoire naturelle (MNHN)
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.

